طراحی دارو با روشهای کامپیوتری و داکینگ ملکولی
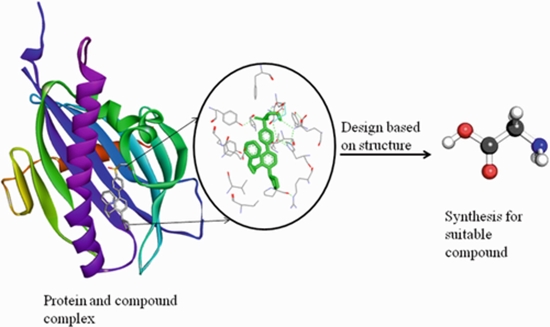
طراحی دارو با روشهای کامپیوتری و داکینگ ملکولی
در دو دهه گذشته، پیشرفتهای چشمگیری در زمینه طراحی دارو به کمک روشهای کامپیوتری و داکینگ ملکولی صورت گرفته است. این روشها به پژوهشگران این امکان را میدهند که فرآیند توسعه دارو را تسریع کرده و هزینهها را کاهش دهند. طراحی دارو بهصورت سنتی زمانبر و پرهزینه بود، اما ابزارهای نوین کامپیوتری بهویژه در زمینه شبیهسازیهای مولکولی و داکینگ، بهطور قابل توجهی این روند را بهبود بخشیدهاند.
تعریف داکینگ ملکولی
داکینگ ملکولی روشی است که در آن تعاملات بین یک لیگاند (مولکول دارویی) و یک هدف بیولوژیکی (معمولاً پروتئین یا آنزیم) شبیهسازی میشود. هدف این فرایند، شناسایی مکان و نحوه اتصال لیگاند به هدف و همچنین ارزیابی پتانسیل بیولوژیکی آن است. با استفاده از داکینگ، پژوهشگران میتوانند به پیشبینی ساختار و ویژگیهای مولکولی داروها بپردازند و در نهایت بهترین ترکیبها را برای آزمایشهای بالینی انتخاب کنند.
مراحل طراحی دارو با داکینگ ملکولی
- شناسایی هدف: نخستین مرحله در طراحی دارو، شناسایی هدف بیولوژیکی است که معمولاً بهعنوان یک پروتئین مهم در یک بیماری خاص شناخته میشود. این مرحله شامل مطالعه ساختار و عملکرد پروتئین و تحلیل مکانیسمهای بیولوژیکی است.
- جمعآوری دادههای ساختاری: پس از شناسایی هدف، دادههای ساختاری مولکول هدف از پایگاههای دادهای مانند Protein Data Bank (PDB) جمعآوری میشود. این دادهها معمولاً شامل ساختار سهبعدی پروتئین و اطلاعات مربوط به توالی آن هستند.
- تولید کتابخانه لیگاند: در این مرحله، مجموعهای از مولکولهای بالقوه دارویی (لیگاندها) تهیه میشود. این مولکولها میتوانند از طریق روشهای مختلفی مانند شیمی محاسباتی، شیمی ترکیبی و یا پایگاههای دادهای از ترکیبات موجود جمعآوری شوند.
- انجام داکینگ: با استفاده از نرمافزارهای داکینگ ملکولی، لیگاندها به پروتئین هدف متصل میشوند و تعاملات احتمالی شبیهسازی میشود. این نرمافزارها با استفاده از الگوریتمهای پیچیده، بهترین حالت اتصال و انرژی آزاد شده از این اتصال را محاسبه میکنند.
- تحلیل نتایج: پس از انجام داکینگ، نتایج بهدستآمده تحلیل میشود. پژوهشگران به بررسی انرژی اتصال، نوع و تعداد تعاملات بین لیگاند و پروتئین میپردازند. این تحلیل به انتخاب لیگاندهای با پتانسیل بالا کمک میکند.
- آزمونهای تجربی: در نهایت، لیگاندهای منتخب به آزمایشگاه منتقل میشوند تا از نظر بیولوژیکی و دارویی مورد ارزیابی قرار گیرند. این مرحله شامل آزمایشهای in vitro و in vivo است تا تأثیرات واقعی دارو بر روی سلولها و موجودات زنده سنجیده شود.
مزایای استفاده از داکینگ ملکولی
- کاهش زمان و هزینه: داکینگ ملکولی میتواند زمان طراحی و توسعه دارو را بهطور قابل توجهی کاهش دهد. با شبیهسازیهای اولیه، پژوهشگران میتوانند تعداد بیشتری از ترکیبات را در مدت زمان کوتاهتری بررسی کنند.
- دقت بیشتر: روشهای کامپیوتری امکان پیشبینیهای دقیقتری را در مورد تعاملات مولکولی فراهم میکنند، که میتواند به انتخاب ترکیبات با ویژگیهای بهینه کمک کند.
- بهینهسازی مجدد: داکینگ ملکولی این امکان را میدهد که ترکیبات جدید از طریق بهینهسازی ساختاری و تغییرات جزئی در لیگاندها طراحی شوند.
چالشها و محدودیتها
با وجود مزایای زیاد، طراحی دارو با استفاده از داکینگ ملکولی نیز با چالشها و محدودیتهایی مواجه است. یکی از بزرگترین چالشها، پیچیدگی و تنوع تعاملات بیولوژیکی است. همچنین، دقت پیشبینی داکینگ بستگی به کیفیت دادههای ورودی و مدلهای مورد استفاده دارد. از طرفی، بسیاری از پروتئینها در حالت طبیعی خود بهصورت دینامیک عمل میکنند و این دینامیکها ممکن است در مدلهای ایستا لحاظ نشود.
نتیجهگیری
طراحی دارو با استفاده از روشهای کامپیوتری و داکینگ ملکولی، انقلابی در علم داروسازی ایجاد کرده است. این روشها به پژوهشگران این امکان را میدهند که با سرعت و دقت بیشتری داروهای جدید را شناسایی و توسعه دهند. با پیشرفتهای مستمر در این زمینه، انتظار میرود که ابزارهای نوین، فرآیند طراحی دارو را بهطور قابل توجهی بهبود بخشند و به کشف درمانهای مؤثرتر برای بیماریهای مختلف کمک کنند

ارسال نظر